依据《医疗器械监督处理条例》的规则,中华人民共和国境内的医疗器械依照危险程度分为三类:第I类、第II类和第III类。
关于第II类医疗器械,它们具有中度危险,需求严控处理以保证其安全、有用的医疗器械。境内出产企业要在所在地省(直辖市)药监局进行注册,而境外医疗器械出产企业要托付境内署理人在国家药监局进行注册。
第III类医疗器械具有较高危险,需求采纳特别办法严控处理以保证其安全、有用的医疗器械。不管境内、境外医疗器械出产企业均需求在国家药监局进行注册。
已注册的第二类、第三类医疗器械产品,假如其规划、原材料、出产的根本工艺、使用范围、使用方法等产生实质性改变,有或许影响该医疗器械安全、有用的,注册人应向原注册部分请求处理改变注册手续。相反,假如产生非实质性改变,不影响该医疗器械安全、有用的,应当将变化状况向原注册部分存案。
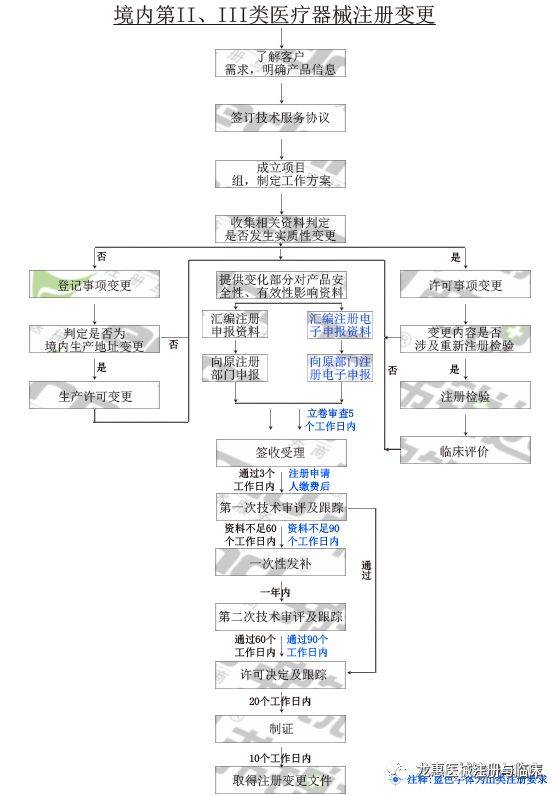
9、《境内第三类医疗器械注册质量处理体系核对作业程序(暂行)》(食药监械管〔2015〕63号)
新闻中心

Copyright © 2013-2014 米乐m6体育官网app下载安装 浙ICP备2021001089号-1 ,主营:乳化泵、高剪切乳化机、减速机支架、乳化罐、釜底乳化机 版权所有网站地图
联系人:佘经理
电 话:0577-86810550
传 真:0577-86814050
手 机:15158693139
Q Q:669453420
友情网站: 米乐m6体育官网 米乐m6下载安装 m6米乐app官网下载